Тихая ошибка системы
Как организм обнаруживает и нейтрализует опасные сбои в собственных клетках.
На примере мутации JAK2 V617F и аллель‑специфичного РНК‑вмешательства.
Пролог. Когда система формально работает
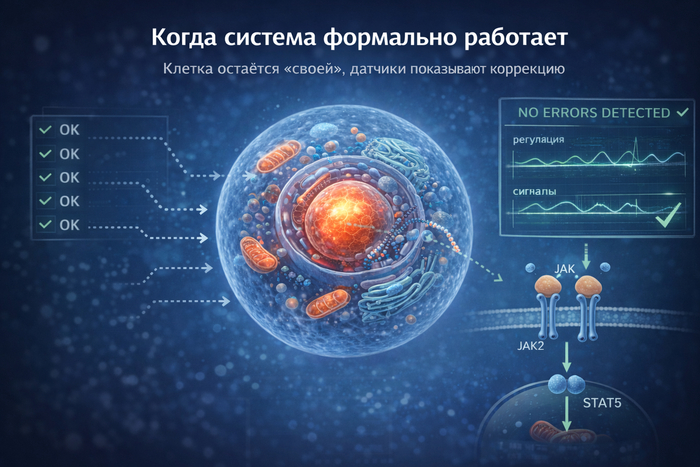
Самые сложные проблемы редко начинаются с аварии. Чаще они выглядят как корректная работа всех компонентов при неправильном общем результате. Датчики не срабатывают, контрольные списки пройдены, тревоги нет — но последствия накапливаются.
В биологии существуют именно такие ситуации. Клетки остаются «своими», инструкции почти не отличаются от нормы, сигнальные пути знакомы. Однако в одном из элементов регуляции возникает устойчивое отклонение. Оно не выглядит как поломка, но со временем меняет поведение всей системы.
Этот текст — разбор такого сбоя. Не борьба с врагом, а анализ внутреннего отклонения и способов его корректного устранения без разрушения системы.
Глава 1. Базовые понятия (кратко и по делу)
Чтобы двигаться дальше, зафиксируем минимальный набор терминов.
ДНК — долговременная инструкция, по которой клетка устроена и функционирует.
Ген — отдельный участок этой инструкции.
мРНК — рабочая копия гена, используемая для сборки белка.
Белок — функциональный элемент: фермент, рецептор, сигнальный узел.
Мутация — изменение в инструкции, которое может быть нейтральным или нарушающим регуляцию.
Принципиально важно: клетка не использует ДНК напрямую. Все решения реализуются через мРНК. Это промежуточный уровень, на котором возможна точечная коррекция без вмешательства в исходный код.
Глава 2. Локальный сбой: что происходит при JAK2 V617F
Белок JAK2 участвует в передаче сигнала роста. В норме он активируется только при наличии внешнего стимула — например, сигнала от факторов роста.
Мутация V617F изменяет одну аминокислоту, но приводит к принципиальному эффекту:
сигнальный путь JAK‑STAT становится активным постоянно;
клетка теряет зависимость от внешних регуляторов;
появляется устойчивое преимущество в делении;
формируется расширяющийся клон таких клеток.
Формально компоненты системы исправны. Фактически нарушено одно правило: активация без разрешающего сигнала.
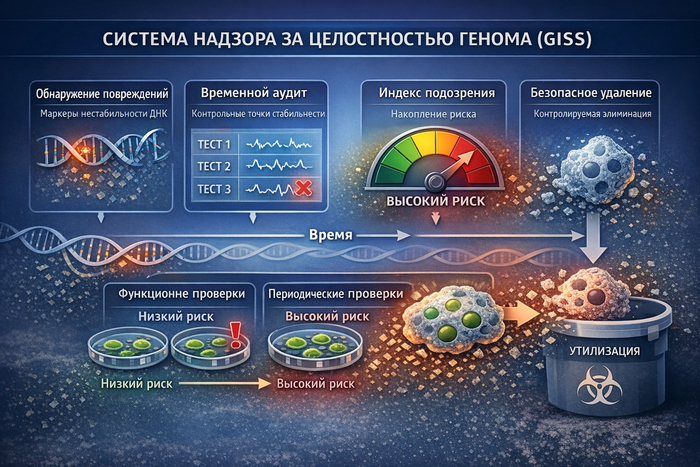
Глава 3. Почему стандартный иммунный контроль не реагирует
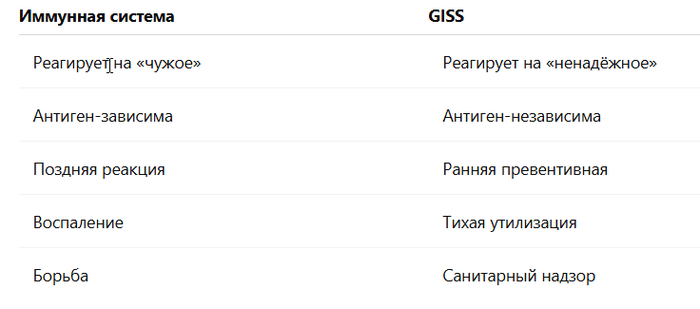
Иммунная система оптимизирована для обнаружения внешних угроз. Её базовый вопрос — есть ли признаки «чужого».
В случае JAK2 V617F:
структура ДНК почти не отличается от нормы;
белок не выглядит инородным;
воспалительный контекст отсутствует.
С точки зрения встроенного контроля — все параметры в допустимых диапазонах. Сбой не классифицируется как угроза, хотя его последствия системны.
Глава 4. Почему жёсткое устранение — неэффективная стратегия
Интуитивное решение — удалить проблемную клетку. Однако в биологических системах прямое уничтожение часто создаёт новые проблемы:
повреждение ткани;
хроническое воспаление;
риск затронуть здоровые клетки, особенно в костном мозге.
Эволюционно более устойчивый подход — не устранять элемент, а лишить его некорректного преимущества и вернуть под общий контроль регуляции.
Глава 5. Диагностический признак: мРНК
Ключевой момент анализа — уровень, на котором сбой становится однозначным.
Мутация JAK2 V617F присутствует в мРНК. В отличие от белков, мРНК:
линейна;
однозначно читается;
отличается от нормальной версии одним нуклеотидом.
С инженерной точки зрения это аналог лог‑файла, в котором ошибка уже зафиксирована, но ещё не привела к необратимым последствиям.
Глава 6. Инструмент точечной коррекции: аллель‑специфичное РНК‑вмешательство
Аллель‑специфичное РНК‑вмешательство позволяет воздействовать не на ген целиком, а только на его патологическую версию.
Логика работы:
Молекула распознаёт мутантную мРНК по точному совпадению.
Связывается с ней.
Блокирует её работу или инициирует деградацию.
Уровень мутантного белка падает.
Нормальный JAK2 продолжает функционировать. Система теряет только некорректный сигнал.
Глава 7. Поведение системы после устранения сбоя
Важно подчеркнуть: клетка не уничтожается принудительно.
После потери автономного сигнала деления:
исчезает конкурентное преимущество;
клетка перестаёт активно размножаться;
она либо вытесняется нормальными клетками, либо переходит в неактивное состояние.
Организм завершает процесс стандартными механизмами обновления тканей.
Глава 8. Подтверждение реализуемости подхода
Подобная стратегия уже используется в медицине. Наиболее известный пример — болезнь Хантингтона.
В этом случае:
мутантный белок токсичен;
нормальный белок необходим;
применяются методы селективного подавления мутантной мРНК.
Это не теоретическая модель, а клинические исследования и поздние фазы испытаний.
Глава 9. Почему клетки крови — подходящая среда
Для кроветворных клеток:
РНК‑препараты можно вводить системно;
мРНК доступна в цитоплазме, без необходимости вмешательства в ядро;
эффекты обратимы и контролируемы по дозе.
Поэтому мутация JAK2 V617F считается одной из наиболее перспективных мишеней для аллель‑специфичных подходов.
Глава 10. Чем этот подход отличается от прежних медицинских стратегий
Это не иммунная активация. Не химиотерапия. Не редактирование ДНК.
Это точечная коррекция регуляции, направленная на восстановление системных правил работы.
Вмешательство минимально, но устраняет ключевое отклонение.
Эпилог. Что дальше и зачем это нужно
Сроки и ожидания
RNA‑терапии уже одобрены для ряда заболеваний;
аллель‑специфичные методы проходят клинические фазы;
для мутаций крови речь идёт о горизонте 5–10 лет.
Зачем развивать этот подход
снижение побочных эффектов;
возможность длительного контроля хронических состояний;
переход от агрессивного лечения к управляемой коррекции.
Итоговая мысль
Будущее медицины всё меньше похоже на войну и всё больше — на точный анализ сложных систем. Важнее не уничтожить элемент, а корректно устранить отклонение, сохранив целостность всей системы.
Анализ завершён. Работа над системой продолжается.
Почему этот подход может изменить медицину
На первый взгляд аллель-специфичное РНК-вмешательство выглядит как ещё один «тонкий инструмент» среди множества биомедицинских технологий. Но если посмотреть шире, становится ясно: речь идёт не об отдельном методе, а о смене логики лечения.
От борьбы с болезнью — к управлению отклонениями
Классическая медицина часто мыслит бинарно:
либо клетка «плохая» и её нужно уничтожить,
либо она «хорошая» и её не трогают.
Но реальная биология устроена иначе. Большинство патологий — это не появление принципиально нового объекта, а небольшое отклонение в работе уже существующей системы.
Аллель-специфичное РНК-вмешательство позволяет работать именно с такими отклонениями, не разрушая систему целиком.
Ключевые моменты
От уничтожения клеток — к устранению нечестного преимущества
Мы не убиваем клетки, а селективно отключаем автономные сигналы роста и позволяем организму завершить процесс.Работа с первопричиной на уровне РНК
Воздействие на мутантные транскрипты выше уровня белков повышает точность и снижает риск резистентности.Аллель-специфичная избирательность
Подавляется патологический вариант, при сохранении нормальной функции гена — ключевое отличие по безопасности.Платформа, а не единичный препарат
Одна архитектура применима к множеству точечных мутаций в онкологии и наследственных заболеваниях.Клинически реалистичный тайминг
РНК-терапии уже одобрены; пути доставки и регуляторные процессы отработаны.Долгосрочная ценность
Подход ориентирован на хроническое управление заболеванием с низкой токсичностью и сильным IP-потенциалом.